Хімічні властивості карбонових кислот багато в чому подібні до властивостей неорганічних кислот. Усі органічні кислоти — слабкі, а більшість не розчиняються у воді.
На хімічні властивості карбонових кислот впливає будова її характеристичної (функціональної) групи. Розглянемо на прикладі етанової кислоти. Характеристична група молекули етанової кислоти карбонових кислот складається з двох груп: гідроксильної і карбонільної . Атом Оксигену, що міститься в складі карбонільної групи, відтягує на себе електронну густину хімічного зв'язку, унаслідок чого зв'язок між атомами Оксигену й Гідрогену в гідроксильній групі послаблюється. Зміщення електронної густини визначає кислотні властивості цієї речовини:
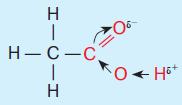
1. Електролітична дисоціація. Розчинні у воді карбонові кислоти дисоціюють з утворенням йонів Гідрогену, змінюючи забарвлення індикаторів, як і слабкі неорганічні кислоти. Але під час дисоціації від молекули карбонових кислот відщеплюється тільки Гідроген карбоксильної групи. Тому основність органічних кислот не збігається з числом атомів Гідрогену, що міститься в її молекулі, а дорівнює числу карбонових кислот:
- у загальному вигляді: ;
- для метанової кислоти: .
Зі збільшенням вуглеводневого залишку сила карбонових кислот зменшується (ступінь дисоціації знижується).
2. Кислотно-основні реакції. Для карбонових кислот характерні всі загальні хімічні властивості кислот. Вони реагують:
- з активними металами: ;
- з основними оксидами: ;
- з лугами: ;
- із солями: .
3. Реакція естерифікації. Естерифікація — реакція утворення естерів під час кип'ятіння карбонових кислот зі спиртами за наявності концентрованої сульфатної кислоти:
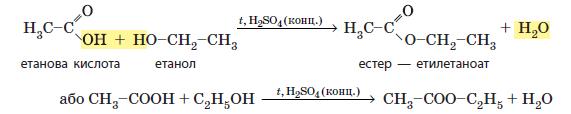
Від карбоксильної групи кислоти відщеплюється група , а від молекули спирту — атом Гідрогену гідроксильної групи. Разом вони утворюють молекулу води, зв'язуванню якої сприяє концентрована сульфатна кислота. У цій реакції вона є і каталізатором, і водовідіймаючим засобом.
4. Реакція галогенування. Карбонові кислоти виявляють певні хімічні властивості й за участі вуглеводневого залишку, що споріднює їх з алканами. Вони взаємодіють з хлором та бромом за наявності фосфор(\(III\)) хлориду чи броміду, причому реакція відбувається за атомом карбону, найближчим до карбоксильної групи.
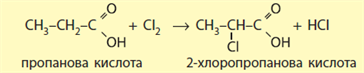
Джерела:
Хімія (рівень стандарту): підруч. для 10 кл. закл. зак. серед. освіти / М.М. Савчин. — Київ: Грамота, 2018. с. 83-84.
Хімія (рівень стандарту): підруч. для 10 класу закл. загал. серед. освіти / О.В. Григорович. — Харків: Ранок, 2018. с. 128-129.
