Отримання водню
- У лабораторії водень отримують взаємодією кислоти з металом, які стоять у ряду активності до . Зазвичай використовують хлоридну або розбавлену сульфатну кислоту і метали середньої активності (цинк або залізо):
,
.
Збирають водень, який виділяється витісненням повітря чи витісненням води:
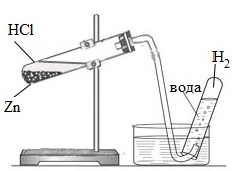
- У промисловості водень отримують конверсією (взаємодією) водяної пари з вугіллям або метаном:
,
.
Застосування водню
- З водню отримують найважливіші хімічні сполуки: амоніак і гідроген хлорид.
- Реакцію горіння водню застосовують для різання і зварювання металів.
- Водень використовується як паливо в ракетних двигунах.
- Воднем можна відновлювати метали з їх оксидів.
- За допомогою водню рідкі жири перетворюють у тверді (рослинну олію — у маргарин).
- Водень застосовується для отримання багатьох органічних речовин.
