1. Повне окиснення. Як і більшість органічних речовин, багатоатомні спирти горять. Продуктами реакції є вуглекислий газ і вода:
У разі нагрівання вище \(300\) °С гліцерол спалахує. Здатність гліцеролу горіти використовують у прозорих свічках.
2. Взаємодія з активними металами. Як і одноатомні, багатоатомні спирти виявляють слабкі кислотні властивості. Гліцерол активно взаємодіє з активними металами, наприклад, з натрієм:
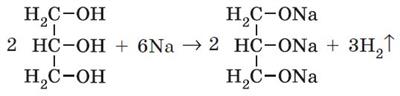
або
Взаємодія гліцеролу з натрієм відбувається дуже бурхливо, з виділенням великої кількості теплоти, унаслідок чого водень, який виділяється, може зайнятися.
3.Реакція з лугами. Гліцерол може взаємодіяти з лугом з утворенням калій гліцерату:
3. Особлива властивість багатоатомних спиртів — реакція з купрум(\(II\)) гідроксидом. У результаті цієї реакції утворюється яскраво-синій розчин, тому вона використовується як якісна реакція на багатоатомні спирти, тобто за допомогою купрум(\(II\)) гідроксиду можна відрізнити багатоатомний спирт від інших речовин:

Якісна реакція на гліцерол
Джерела:
Хімія (рівень стандарту): підруч. для 10 класу закл. загал. серед. освіти / О.В. Григорович. — Харків: Вид-во «Ранок», 2018. с. 99-100.
