Силікатна (кремнієва) кислота — дуже слабка, нерозчинна у воді кислота. Її отримують у вигляді драглистого осаду при дії сильних кислот на розчини силікатів:
.
Силікатна кислота є настільки слабкою, що її можна витіснити з солей навіть карбонатною кислотою:
.

Натрій силікат + хлоридна кислота
Гелеподібний осад силікатної кислоти через деякий час стає густим і заповнює увесь об'єм посудини.

Осад силікатної кислоти, що загуснув
Особливості властивостей силікатної кислоти пояснюються її будовою. Силікатна кислота не має постійного складу, тому замість формули інколи використовують запис . Кислота має полімерну будову:
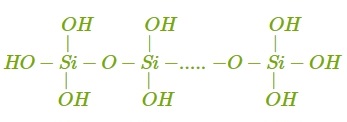
Силікатна кислота нестійка і при тривалому зберіганні або підвищеній температурі розкладається на воду і силіцій(\(IV\)) оксид:
.
Силіцій(\(IV\)) оксид утворюється у вигляді пористої твердої речовини — силікагелю.
Силікатна кислота не розчиняється у воді, не дисоціює, не змінює забарвлення індикаторів. Як і всі кислоти, вона реагує з основними і амфотерними оксидами і гідроксидами. У результаті реакцій утворюються солі силікати (, ).
З силікатів розчинні лише солі лужних металів, і їх називають розчинним або рідким склом. Силікати натрію і калію входять до складу силікатного клею.
Концентровані розчини цих солей використовуються для просочення дерев'яних виробів і тканин з метою надання їм вогнетривких властивостей. При висиханні силікати утворюють склоподібний шар, який не пропускає воду, тому застосовуються і в якості водовідштовхувальних покриттів.

У природі зустрічаються силікати і алюмосилікати. До них належать граніт, слюда, азбест, глина. Ця доступна сировина давно освоєна людиною і широко використовується у будівництві.
Глина легко формується, при спіканні стає твердою, тому вона застосовується для виготовлення керамічних виробів.

Глиняний посуд

Фарфоровий посуд

Цегла керамічна
При нагріванні глини з вапняком отримують найважливіший будівельний матеріал — цемент.

Цемент