При нормальних умовах основи (гідроксиди металів) є твердими кристалічними речовинами. Вони нелеткі і не мають запаху.
Розчинність основ у воді
За розчинністю у воді ці сполуки ділять на дві групи: луги і практично нерозчинні основи . У свою чергу, луги ділять на добре розчинні у воді і малорозчинні основи.
Загальновстановлених, чітких меж між добре розчинними, малорозчинними і практично нерозчинними у воді речовинами не існує, тому довідкові дані, взяті з різних джерел, можуть дещо відрізнятися одні від одних. Наведемо відомості про розчинність лугів, яких ми дотримуватимемося.
Класифікація лугів за їх розчинністю у воді:
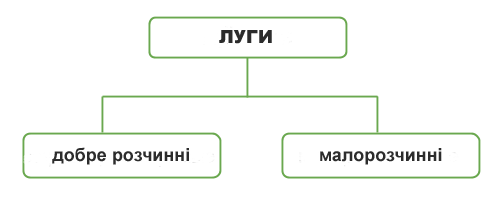
— літій гідроксид — натрій гідроксид — калій гідроксид — рубідій гідроксид — цезій гідроксид — францій гідроксид — барій гідроксид — радій гідроксид | — кальцій гідроксид — стронцій гідроксид |
Зверни увагу!
Майже всі інші основи (гідроксиди металів) є практично нерозчинними.
Забарвлення основ
Більшість основ — речовини білого кольору. Проте, існують гідроксиди металів, які мають забарвлення.Колір основи | Приклади |
Білий | — літій гідроксид — магній гідроксид — кальцій гідроксид |
| Жовтий | — купрум(\(I\)) гідроксид |
Світло-рожевий (при контакті з киснем повітря забарвлення стає коричневим) | — манган(\(II\)) гідроксид |
| Червоно—коричневий | — ферум(\(III\)) гідроксид |
Білий з зеленуватим відтінком (при контакті з киснем повітря забарвлення стає темнішим) | — ферум(\(II\)) гідроксид |
| Світло зелений | — нікель(\(II\)) гідроксид |
| Синій | — купрум(\(II\)) гідроксид |