Основами називають складні речовини, до складу яких входять металічні хімічні елементи, сполучені з однією або декількома гідроксогрупами (групами атомів \(— OH\)).
Виходячи з цього, загальну хімічну формулу основ можна зобразити наступним чином:
,
де \(M\) — знак металічного хімічного елемента,
а \(n\) — індекс, чисельно співпадаючий з валентністю металу.
Номенклатура основ
Назва основи складається з назви металічного хімічного елемента у називному відмінку і слова «гідроксид». Якщо металічний елемент має змінну валентність, то вона вказується римськими цифрами в дужках без пробілу одразу після назви металу.
Приклад:
— натрій гідроксид,
— ферум(\(II\)) гідроксид,
— ферум(\(III\)) гідроксид.
Класифікація основ
Зверни увагу!
Основи класифікують за двома ознаками — розчинністю у воді, і кількістю гідроксильних груп.
Розчинні у воді основи називають лугами.
За їх здатністю розчинятися у воді основи ділять на розчинні і практично нерозчинні:
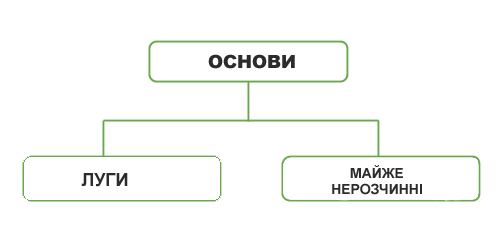
|
Приклади:
— натрій гідроксид
— калій гідроксид
— кальцій гідроксид
|
Приклади:
— купрум(\(II\)) гідроксид
— ферум(\(II\)) гідроксид
— ферум(\(III\)) гідроксид
|
Кислотність основ
За числом гідроксильних груп основи бувають однокислотні (, , ), двокислотні ( , , ), багатокислотні ().