Запропонована Е. Резерфордом у \(1911\) році ядерна (планетарна) модель будови атома зводиться до наступних положень:
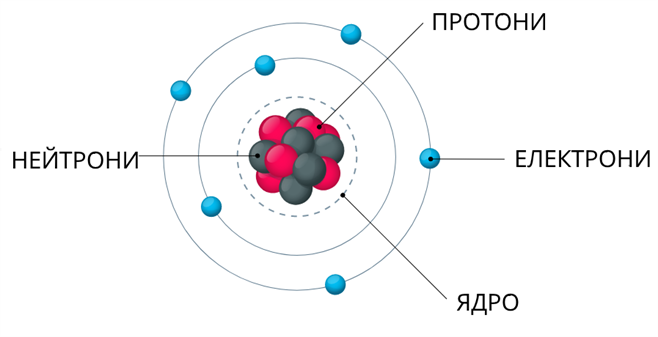
• атом складається з позитивно зарядженого ядра і електронів, що рухаються навколо нього;
• більше \(99,96\) % маси атома зосереджена в його ядрі;
• діаметр ядра приблизно в сто тисяч разів менше діаметра самого атома.
Відповідно до цієї моделі можна дати наступне визначення атома:
Атом — електронейтральна частинка, що складається з позитивно зарядженого ядра і негативно заряджених електронів.
Ядро атома складається з елементарних частинок: протонів і нейтронів. Протони і нейтрони мають загальну назву нуклони (ядерні частинки).
Протон (\(p\)) — частинка, яка має заряд \(+1\) і відносну масу, що дорівнює \(1\).
Нейтрон (\(n\)) — частинка без заряду і відносною масою \(1\).
До елементарних частинок відносяться також електрони (\(e\)), які утворюють електронну оболонку атома.
Протони і нейтрони мають однакову масу. Маса електрона складає маси протона і нейтрона. Тому основна маса атома зосереджена в його ядрі.
Протон має позитивний заряд \(+1\). Заряд електрона — негативний і по величині дорівнює заряду протона \(–\)\(1\).
|
Частинки
|
Відносна
маса
|
Відносний
заряд
|
| Протон |
1
|
+1
|
| Нейтрон |
1
|
0
|
| Електрон |
1/1840
|
–1
|
Встановлено, що число протонів в ядрі дорівнює порядковому номеру елемента в періодичній таблиці.
Заряд ядра визначається числом протонів в ньому. Отже, заряд ядра теж дорівнює порядковому номеру елемента.
Атом — електронейтральна частинка, тому число електронів в ньому дорівнює числу протонів.
Зверни увагу!
Порядковий номер элемента \(=\) заряду ядра атома \(=\) числу протонів у ядрі \(=\) числу електронів в атомі.
Гідроген — елемент № \(1\). Заряд ядра його атома дорівнює \(+1\). В ядрі знаходиться один протон, а в електронній оболонці — один електрон.
Карбон — елемент № \(6\). Заряд ядра його атома дорівнює \(+6\), у ньому — \(6\) протонів. В атомі міститься \(6\) електронів з загальним зарядом \(–\)\(6\).
Зверни увагу!
Заряд ядра — головна характеристика атома.
Вивчення будови атомних ядер привело до уточнення формулювання періодичного закону. Сучасне формулювання звучить наступним чином:
Властивості хімічних елементів і утворених ними простих і складних речовин перебувають у періодичній залежності від величин зарядів ядер їх атомів.
